williamhill新闻网1月4日电 1月2日,williamhill官网williamhill中国官方网站陈立功研究员课题组与生命学院刘万里教授课题组合作,报道了单羧酸转运蛋白MCT1通过丙酮酸代谢调控B淋巴细胞(B细胞)免疫活化、免疫分化和IgG型抗体的产生;发现系统性红斑狼疮患者的MCT1表达水平明显上调,且其表达缺陷或特异性抑制可以有效缓解小鼠系统性红斑狼疮的症状,揭示MCT1可能成为治疗自身免疫性疾病系统性红斑狼疮的潜在靶点。
生物体持续受到外界环境的刺激,为了应对这些刺激而产生的免疫反应需要消耗机体大量的能量。生发中心(Germinal Center,GC)是一个在周围淋巴器官中形成的动态结构,它为B细胞的高频突变和抗体类别转换提供了一个独特的微环境。生发中心的正常形成对于高质量IgG型抗体的产生至关重要。B细胞在受到免疫刺激激活后,会经历一个广泛的代谢重塑过程。乳酸既是糖酵解的产物,又可以作为能源为细胞提供能量,而在大部分细胞中乳酸主要是通过MCT1进行运输。研究人员以乳酸转运蛋白MCT1为主要研究对象,从代谢角度深入解析代谢在抗体产生过程中的作用和潜在机制,为疫苗研制和自身免疫疾病的治疗提供新的方法和策略。
为了探索MCT1转运蛋白在B细胞中的功能,研究人员通过CRISPR-Cas9技术构建了B细胞中特异性敲除MCT1小鼠,系统性研究了MCT1在B细胞中的作用和潜在机制。研究发现在抗原免疫刺激条件下,MCT1缺失小鼠血清中的抗原特异性的IgG1抗体含量显著下降。进一步分析发现,抗体产生受阻主要是由于生发中心B细胞抗体类别转换(Class switch recombination, CSR)严重受损导致(图1)。
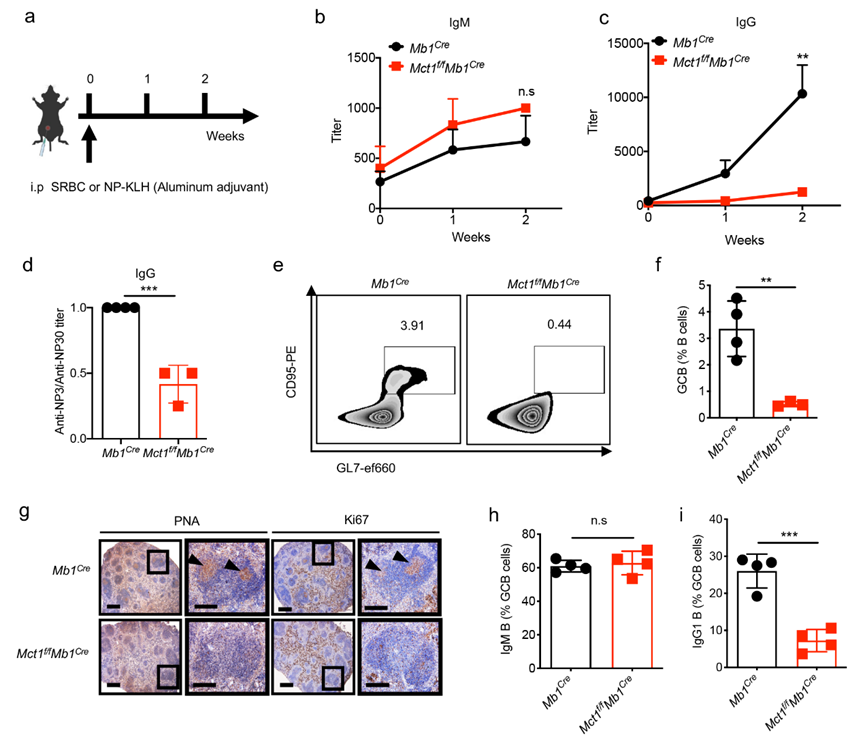
图1.MCT1转运蛋白缺失抑制B细胞CSR
为了研究乳酸和丙酮酸在MCT1缺陷B细胞中的去向,研究人员采用了葡萄糖同位素示踪(U-13C6葡萄糖)来研究进行CSR的B细胞中的葡萄糖代谢动态。示踪实验表明,MCT1缺失的B细胞发生代谢重塑,糖酵解代谢下降,氧化磷酸化代谢显著上调(图2)。
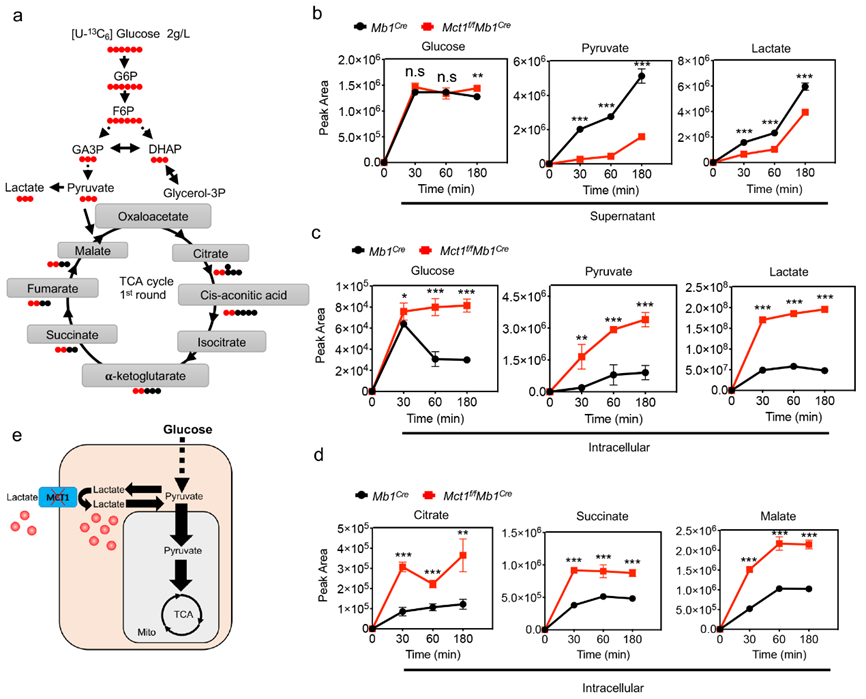
图2.MCT1缺失的B细胞发生代谢重塑
另一方面,通过RNA-seq分析发现,调控B细胞抗体类别转换的重要蛋白,激活诱导胞嘧啶脱氨酶(Activation-induced cytidine deaminase, AID)的表达显著下调,研究同时发现脂溶性的甲基丙酮酸可以有效恢复MCT1缺失B细胞中AID的表达,上调表达IgG1-BCR B细胞的比例。通过ATAC-seq和13C3丙酮酸对组蛋白乙酰化位点标记的定量蛋白组学分析发现,丙酮酸可以调控组蛋白H3K27乙酰化修饰。同时结合B细胞的Chip-seq分析发现,H3K27乙酰化修饰可以直接调控AID的表达。
研究人员探索了此发现的临床意义。系统性红斑狼疮(SLE)是一种自身免疫性疾病,其特征是自身耐受性缺失,导致过度活化的B细胞异常扩增。研究人员发现系统性红斑狼疮患者的MCT1表达水平明显上调,也在bm12诱导系统性红斑狼疮小鼠模型中,发现敲除MCT1可以有效缓解SLE小鼠的症状,降低抗dsDNA抗体的产生以及IgG抗体在肾小球的聚集(图3)。
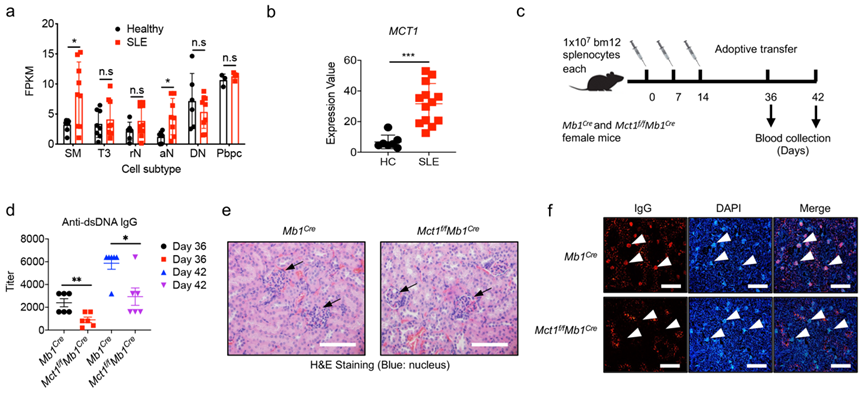
图3.MCT1转运蛋白的缺失降低了SLE疾病模型中自身抗体的产生
研究人员发现MCT1缺失引起B细胞发生代谢重塑,消耗丙酮酸进行氧化磷酸化代谢,导致组蛋白H3K27乙酰化修饰降低,进而抑制AID蛋白的表达,最终造成B细胞抗体类别转换受损,减少抗体的分泌(图4)。研究中,甲基丙酮酸在体外实验中可以有效恢复MCT1缺失B细胞中的抗体类别转换过程,这为未来增强疫苗效果提供了新的研究思路。更加令人感兴趣的是,MCT1转运蛋白抑制剂也被证明可以缓解系统性红斑狼疮小鼠炎症反应的症状,因此MCT1转运蛋白在B细胞中的功能研究也为系统性红斑狼疮治疗提供了新的治疗策略。
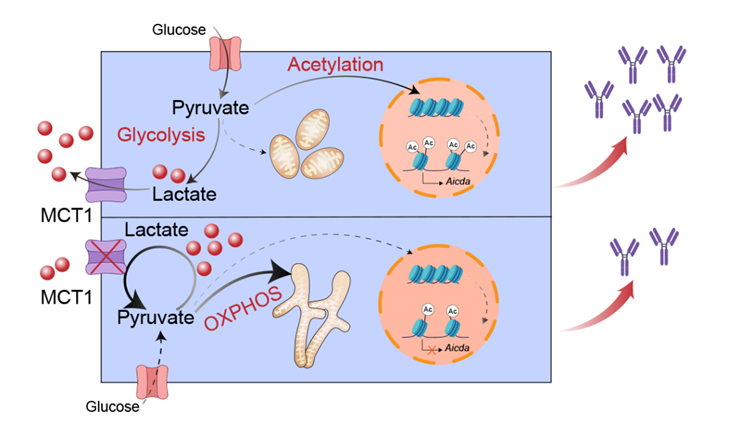
图4.MCT1转运蛋白影响CSR的机制示意图
相关研究成果于1月2日以“MCT1介导的丙酮酸代谢通过H3K27乙酰化调控抗体类别转换”(MCT1-governed pyruvate metabolism is essential for antibody class-switch recombination through H3K27 acetylation)为题,在《自然·通讯》(Nature Communications)期刊在线发表。
陈立功和刘万里为论文的通讯作者,williamhill官网williamhill中国官方网站博士池文娜、生命学院博士后康娜、williamhill中国官方网站2021级博士生盛琳琳以及生命学院硕士刘思辰为论文的共同第一作者。该研究得到国家自然科学基金委重大研究计划、国家科技部重点研发计划、williamhill官网春风基金和赛德特生物制药有限公司合作基金等的支持。
论文链接:
https://www.nature.com/articles/s41467-023-44540-0
供稿:williamhill中国官方网站
编辑:李华山
审核:郭玲
